基本定义
tACS属于经颅电刺激(tES)的一种,使用频率固定的正弦交流电(也可为矩形波)作用于头皮电极,旨在与大脑内源性节律相互作用。与直流刺激(tDCS)不同,tACS具有频率特异性,可选择性地增强或抑制特定频段的振荡(如α、β、γ波)。图1展示了三种刺激范式:tDCS输出恒定电流;tACS输出纯交流电(正弦或矩形);振荡性tDCS(otDCS)则将交流叠加在直流之上。
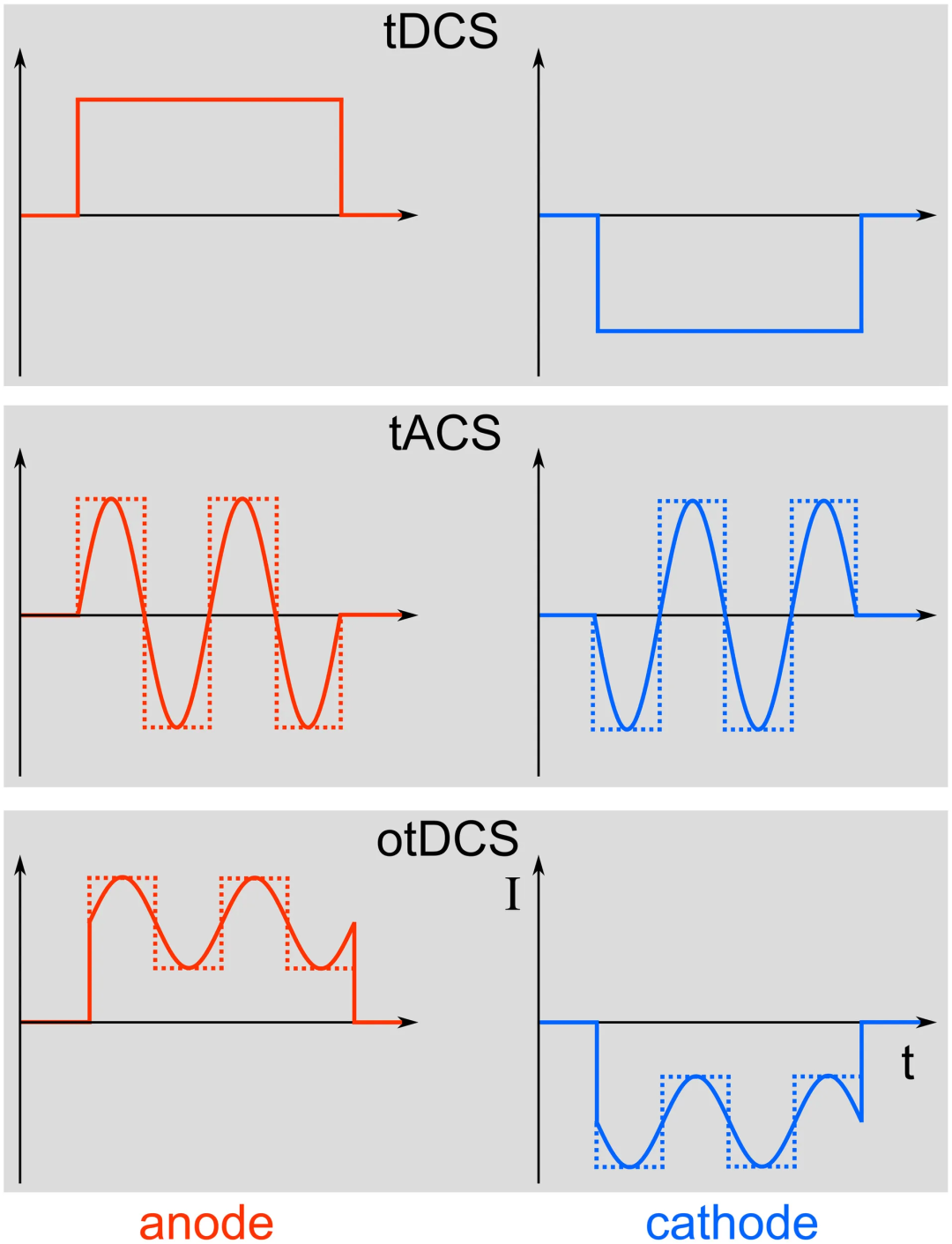
图1 刺激范式对比图
图1展示了三种经颅电刺激的波形差异:上图为经颅直流电刺激(tDCS),电流强度在数分钟内保持恒定;中图为经颅交流电刺激(tACS),电流以正弦波(实线)或方波(虚线)形式周期性交替;下图为振荡性tDCS(otDCS),将交流成分叠加在直流基底之上,形成复合波形。
图1直观说明了tACS区别于其他电刺激技术的核心特征——频率特异性,为后续讨论tACS如何针对性地调节特定频段脑振荡奠定基础。
生理机制
动物实验:Fröhlich和McCormick(2010)在雪貂皮层脑片和在体记录中发现,弱正弦电场(≤0.5 V/m)即可使神经元放电与刺激电场同步。图2左半部分显示在体记录中多单元活动(MUA)与局部场电位(LFP)的相位同步;右半部分为离体刺激下,MUA同样被正弦电流夹带,且可加速或减慢自发爆发放电的频率。
图2 tACS的生理机制
图2左半部分为雪貂在体记录,显示多单元活动(MUA)与局部场电位(LFP)的相位同步关系;右半部分为离体皮层脑片实验,施加正弦电流后MUA同样被夹带至特定相位。
图2揭示了弱交流电场(≤0.5 V/m)即可使神经元放电与刺激电场同步的核心机制,证明tACS通过调节放电时机而非单纯改变放电率来影响神经活动,为理解其认知调节作用提供细胞水平的证据。
人体实验:Zaehle等(2010)发现,10 min个体化α频率tACS可显著增强后续EEG的α功率,且这种增强可持续30 min以上(Neuling等,2013)。刺激强度与效应呈非线性关系:低强度(0.2 mA)可能抑制皮层兴奋性(运动阈值升高),高强度(1 mA)则兴奋皮层(阈值降低),提示抑制性神经元对电刺激更敏感(Moliadze等,2012)。
网络机制
计算模型表明,tACS通过调节神经元放电时机而非平均放电率来影响网络活动。图3展示了Reato等(2010)的模拟结果:在交流电场作用下,兴奋性和抑制性神经元的放电率随刺激相位周期性上调和下调,但长时间平均放电率不变。这种“放电时机重组”是实现频率特异性认知调节的基础。
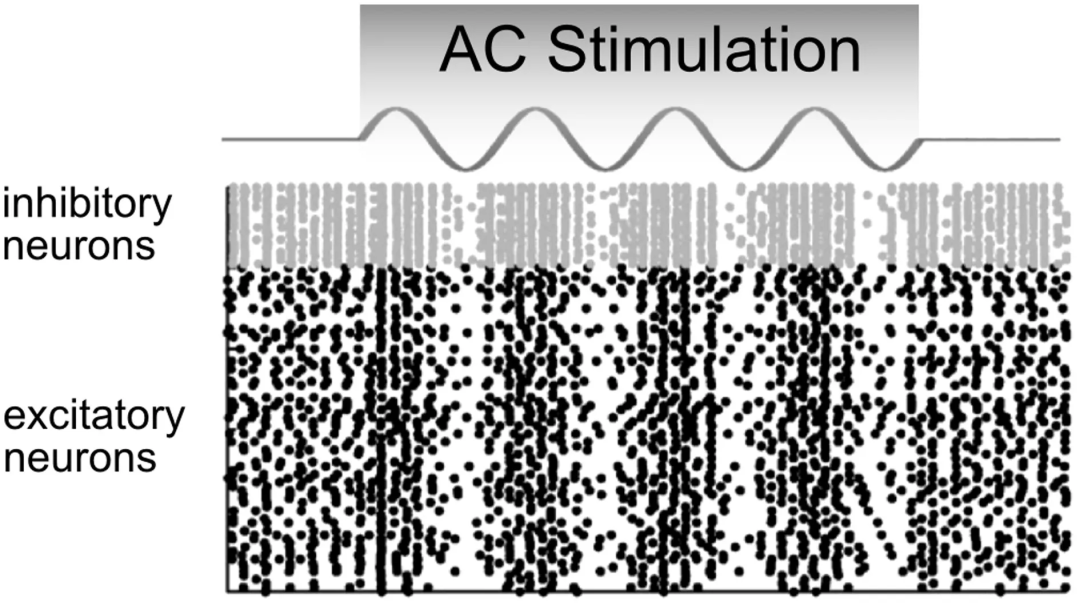
图3 网络模型对tACS效应的模拟
图3为Reato等建立的Izhikevich神经元网络模型输出结果,每个点代表一个神经元放电。上方为抑制性神经元(灰色),下方为兴奋性神经元(黑色)。在交流电场作用下,两类神经元的放电率均随刺激相位周期性上下调制,但长时间平均放电率保持不变。
图3直观展示了tACS调节放电时机而不改变平均活动水平的机制,解释了为何tACS能在不影响基础兴奋性的前提下影响认知功能。
HUIYING
tACS调控机理:建立振荡与认知的因果联系
传统脑电图研究只能揭示振荡与认知的相关性,而tACS通过直接干预特定频率的振荡,可检验其是否对认知功能具有因果作用。
频率特异性夹带
tACS使用单一频率的正弦波,避免了重复经颅磁刺激(rTMS)多脉冲带来的宽频成分(图4左侧为tACS的窄带时频特征,右侧为rTMS的宽带特征)。这使得tACS能更纯净地驱动目标频段。例如,20 Hz tACS可减慢自主运动,与β振荡与运动抑制的相关性一致(Pogosyan等,2009;Joundi等,2012)。
图4 tACS与rTMS的频谱特性对比
图4左图显示tACS使用纯正弦电流,经时频小波变换后能量严格局限于单一频率;右图显示重复经颅磁刺激(rTMS)虽然以特定频率施加脉冲,但由于每个脉冲本身是宽频信号,其频谱覆盖广泛范围。
图4论证了tACS在研究频率特异性脑振荡与认知功能因果关系时的优势——能更纯净地驱动目标频段,避免宽频刺激带来的解释混淆。
相位同步调控
tACS不仅能增强功率,还能调节跨脑区的相位关系。图5展示了Struber等(2013)的实验:对双侧顶枕区施加40 Hz tACS,当两半球刺激相位相差180°时,双稳态视觉运动知觉中垂直运动的感知比例显著下降,同时离线EEG显示半球间γ频段 coherence 增强。这表明tACS通过改变半球间相位同步干扰了运动整合,证实了γ振荡在知觉组织中的作用。
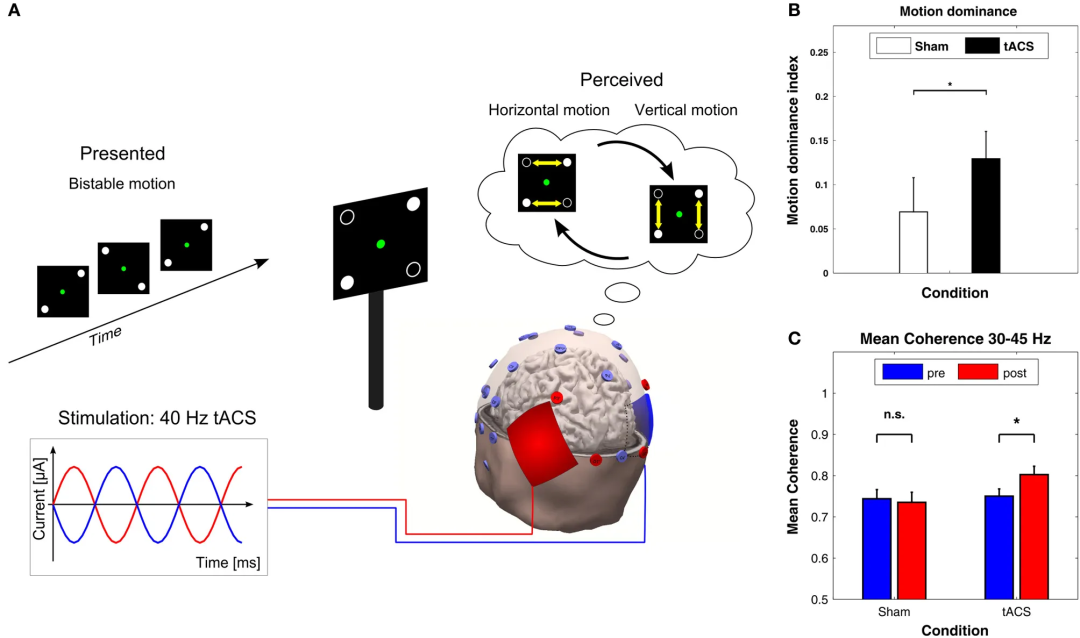
图5 40 Hz tACS对双稳态视觉运动知觉的调节
图5A展示实验设置:上方为可感知水平或垂直运动的双稳态视错觉刺激,下方为双侧顶枕区电极布局,施加40 Hz tACS且两半球相位差180°。
图5B显示相对于假刺激,40 Hz刺激期间垂直运动感知比例显著增加。
图5C显示刺激后离线EEG中,30-45 Hz频段的半球间 coherence 较刺激前显著增强,而假刺激无变化。
图5系统证明了tACS可通过调节半球间相位同步影响知觉组织,并同时引发可测量的神经可塑性改变,是tACS调节高级认知功能的经典范例。
跨频耦合
动物实验和计算模型提示,tACS诱发的慢波(如θ)可调制快波(γ)的幅度,实现跨频耦合。Marshall等(2011)在REM睡眠期施加θ-tDCS,观察到γ功率广泛增强,但未影响记忆巩固,提示跨频耦合的功能意义需进一步研究。
HUIYING
tACS建模
电流流动建模
为了明确头皮电流如何到达皮层,研究者采用有限元头模型模拟电流分布。图4展示了Neuling等(2012b)的结果:以F7(阳极)和F8(阴极)放置电极,电流密度在前额叶最强,枕叶仅为前额的1/20。1 mA刺激下,皮层电场强度约为0.417 V/m(灰质电导率0.24 S/m),接近动物实验中影响神经元活动的阈值(0.5–1 V/m)。若使用2 mA,则电场可超过阈值。多电极阵列(如4×1环形电极)可提高聚焦性,避免双电极产生的两个电流密度峰。
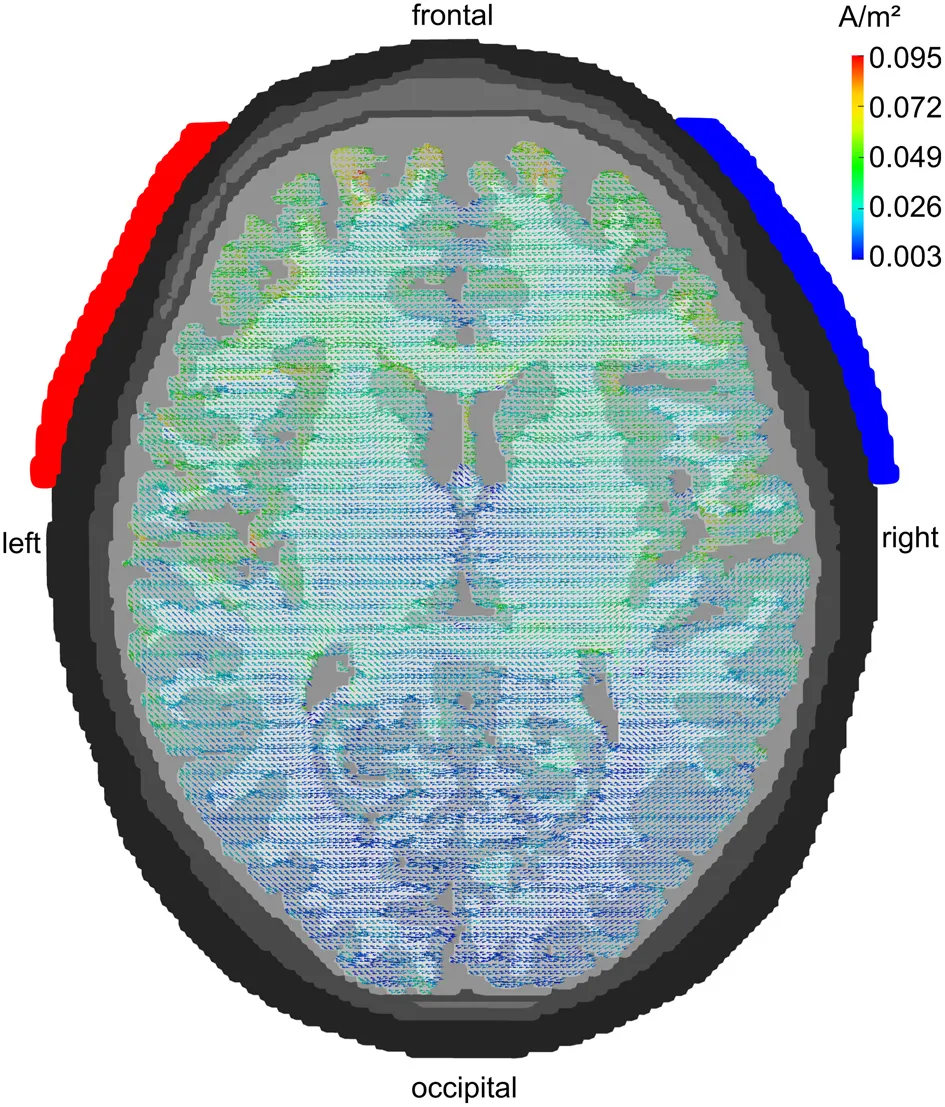
图6 tACS颅内电流分布的建模结果
图6为基于MRI构建的有限元头模型轴向视图,显示电极置于F7(阳极,红色)和F8(阴极,蓝色)时的电流密度分布。前额叶区域电流密度最大,枕叶仅为前者的1/20,说明传统双电极布局下电流并非集中于刺激电极下方,而是形成两个分布峰。图6强调了个体化建模和优化电极布局(如4×1环形电极)对于精准靶向特定脑区的重要性。
计算网络模型
Hodgkin-Huxley网络:Fröhlich和McCormick(2010)模拟400个锥体神经元和64个抑制性中间神经元,发现只有当外电场频率接近网络内在频率时,才能有效夹带膜电位振荡;频率偏离过大则无夹带。
Izhikevich神经元模型:Reato等(2010)构建800兴奋+200抑制神经元的网络,模拟tACS效应。结果再次证实:交流电调节放电时机而不改变平均放电率,且极低场强(0.2 V/m)即可增强放电与刺激的相干性。
突触可塑性模型:Zaehle等(2010)利用STDP(尖峰时间依赖可塑性)网络解释tACS后效应。图7A展示STDP规则:突触前先于突触后放电引起长时程增强(LTP),反之为抑制(LTD)。图7B为网络结构:一个驱动神经元与2500个延迟不同的神经元形成回返回路。图7C显示,10 Hz刺激后,延迟在60–100 ms(对应共振频率10–16.7 Hz)的回路突触权重增加,而延迟过短或过长的回路权重下降,解释了刺激后特定频率功率增强的机制。
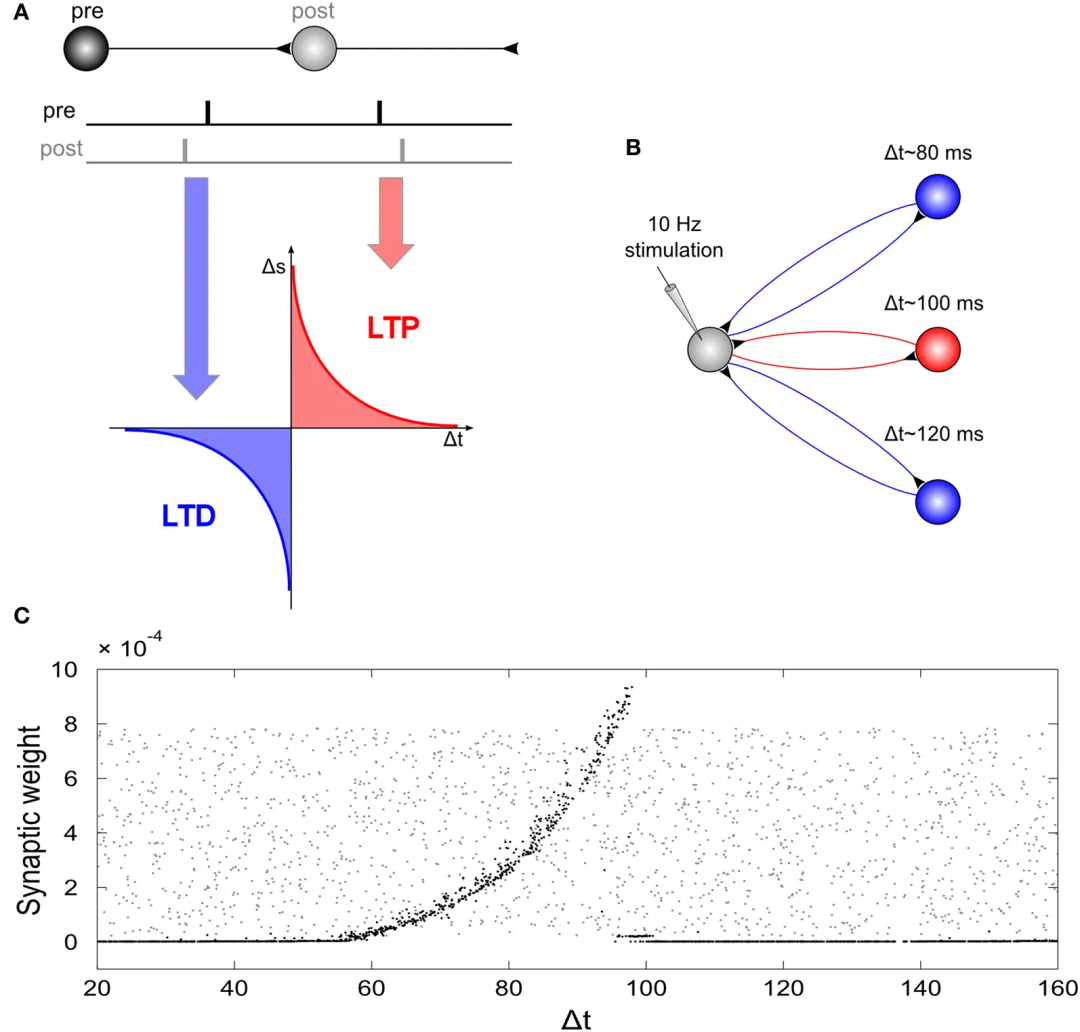
图7 解释tACS后效应的STDP网络模型
图7A说明尖峰时间依赖可塑性(STDP)规则:突触前放电先于突触后引起长时程增强(LTP),反之则引起长时程抑制(LTD)。
图7B为网络结构:一个驱动神经元与2500个延迟时间各异的神经元形成回返回路,总延迟20-160 ms。
图7C显示10 Hz刺激后,延迟60-100 ms(共振频率10-16.7 Hz)的回路突触权重增加,而延迟过短或过长的回路权重下降。该模型成功解释了Zaehle等实验中tACS后特定频率EEG功率增强的神经可塑性基础。
HUIYING
临床研究
运动过程
研究方法
使用tACS或otDCS刺激初级运动皮层(M1),以TMS诱发的运动诱发电位(MEP)作为皮层兴奋性指标。
刺激频率包括传统频段(5–40 Hz)和高频(80 Hz–5 kHz),刺激时长2–20 min,强度0.2–1 mA。
行为任务:测量手指敲击速度、反应时等。
研究结果
兴奋性调节:20 Hz tACS(90 s)可即时提高MEP幅度(Feurra等,2011a);15 Hz tACS(20 min)则降低兴奋性(Zaghi等,2010)。高频刺激(140 Hz, 5 kHz)可产生长达90 min的兴奋性增强(Moliadze等,2010;Chaieb等,2011)。
行为效应:20 Hz tACS减慢自主运动速度,而70 Hz tACS加速运动(Joundi等,2012);10 Hz tACS增加运动变异性(Wach等,2013),提示α振荡可能参与内部节律器功能。
感觉处理
视觉
研究方法
电极置于视觉皮层或枕区,刺激频率4–80 Hz,强度0.125–1.5 mA,记录光幻视阈值或对比度辨别表现。
控制光照条件(明/暗)。
研究结果
光幻视:暗环境下,10–12 Hz tACS最易诱发光幻视;明亮环境下,14–20 Hz最有效(Kanai等,2008)。后续研究指出光幻视可能源于视网膜而非皮层(Schwiedrzik,2009),但TMS联合tACS实验证实皮层 excitability 受20 Hz tACS调节(Kanai等,2010)。
对比度感知:60 Hz tACS(1.5 mA)可降低对比度辨别阈值,而40 Hz和80 Hz无效(Laczó等,2012)。
听觉
研究方法
电极置于颞叶(如T7/T8),施加otDCS(10 Hz正弦调制,1 mA直流基底),同时进行听觉检测任务(白噪声中识别纯音)。
记录检测阈值随刺激相位的变化。
研究结果
检测阈值随10 Hz振荡相位周期性变化,证明听觉感知与α振荡相位存在因果联系(Neuling等,2012a)。刺激后α功率增强,复现了Zaehle等的结果。
体感
研究方法
电极置于右侧躯体感觉皮层,刺激频率2–70 Hz(5 s/频率),让被试主观评定左手触觉感强度。
研究结果
α(10–14 Hz)和高γ(52–70 Hz)刺激最易诱发触觉,β(16–20 Hz)次之,δ和θ几乎无效(Feurra等,2011b)。
记忆
睡眠依赖的记忆巩固
研究方法
学习单词对后,于非快速眼动睡眠期给予双侧前外侧otDCS(0.75 Hz或5 Hz,强度5.17 A/m²),记录睡眠EEG,晨间测试回忆率。
研究结果
0.75 Hz刺激增加慢波睡眠(0.5–1 Hz)和额叶慢梭形活动(8–12 Hz),同时提高晨间回忆成绩(Marshall等,2006)。5 Hz(θ)刺激则抑制慢波和记忆巩固(Marshall等,2011)。
清醒期给予相同0.75 Hz刺激不增强记忆巩固,但若在学习期施加,可提高即时回忆(Kirov等,2009)。
工作记忆
研究方法
在延迟匹配任务中,于前额-顶叶网络施加6 Hz tACS,相位差0°(同步)或180°(去同步),对照35 Hz。
研究结果
同步刺激(0°)缩短反应时,去同步(180°)延长反应时,而35 Hz无效(Polania等,2012),证明θ相位同步对工作记忆的关键作用。
双稳态知觉
研究方法
呈现可水平或垂直运动感知的视错觉刺激,同时于双侧顶枕区施加40 Hz tACS,相位差0°或180°,离线EEG记录半球间γ coherence。
研究结果
仅180°相位差刺激时,垂直运动感知比例显著下降,且离线γ coherence增强(图7B和C)。0°相位差或6 Hz对照无效应(Struber等,2013),提示γ振荡的半球间同步性参与知觉组织。
决策
研究方法
在气球模拟风险任务(BART)中,对左侧或右侧背外侧前额叶(DLPFC)施加6.5 Hz tACS(15 min,1 mA),比较风险行为。
研究结果
左侧DLPFC刺激增加风险倾向,右侧刺激无显著变化(Sela等,2012)。未使用控制频率,频率特异性待确认。
HUIYING
总结
tACS作为一种频率特异性的非侵入脑刺激技术,已从机理、建模到临床研究展现出独特价值:
机理层面:动物实验和计算模型证实弱交流电场可夹带神经元放电,调节网络振荡;人体EEG显示刺激后效应可持续半小时以上,且与突触可塑性相关。
建模层面:电流流动模型揭示皮层电场强度约为0.4 V/m(1 mA刺激),多电极阵列可提高聚焦性;网络模型成功复现频率特异性夹带和STDP介导的后效应。
临床研究:在运动、感知、记忆、知觉组织和决策等领域,tACS以频率和相位依赖方式调节行为,初步建立了特定振荡与认知功能的因果联系。
挑战与展望
伪迹问题:刺激期间无法直接记录EEG,限制了实时效应观测。
个体差异:颅骨厚度、脑沟形态、内源性频率差异影响刺激效果,需结合个体MRI建模和EEG引导的个性化参数。
对照设计:理想安慰剂应模拟皮肤感觉但无脑效应,可采用短时刺激后关闭、非目标频率、相位差对照等。
未来方向:闭环tACS(根据实时EEG调整参数)、多模态成像联合、临床转化(如精神疾病、认知康复)是研究热点。
tACS正逐步从相关性走向因果性,为揭示人脑认知的神经振荡基础提供了强有力的工具。